사람, 동물 유래 검체를 체외에서 검사하고자 단독·조합하여 사용되는 시약, 대조·보정물질, 기구·기계·장치, 소프트웨어 등의 체외진단의료기기!
어떤 절차로 허가되고 있을까요? 등급에 따른 허가 절차 한눈에 알아보아요!
◆ 체외진단의료기기란?
사람이나 동물 유래 검체를 체외에서 검사하기 위해 단독 또는 조합하여 사용되는 시약, 대조·보정물질, 기구·기계·장치, 소프트웨어 등의 의료기기
1. 생리·병리학적 진단
2. 질병의 소인·예후 관찰
3. 선천적 장애 정보 제공
4. 수혈·장기·골수 이식 정보
5. 치료 반응 및 결과 예측
6. 치료적 선택, 효과 모니터링
Q. 1등급 신고 어떤 절차로 진행되나요?
1등급 신고 (신청 : 기술문서 심사 불필요) → 한국의료기기 안전정보원 → 신고증
Q. 2등급 인증·허가 어떤 절차로 진행되나요?
[2등급 인증] 동등공고 제품/동등·개량 제품(임상자료 불필요) → 한국의료기기 안전정보원 → 인증서
[2등급 허가] 새로운 제품·개량제품(임상자료 필요) → 식품의약품안전처 → 허가증
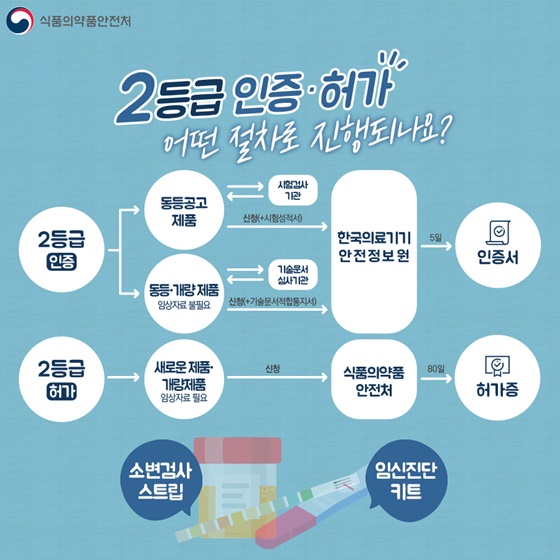
Q. 3·4등급 허가 어떤 절차로 진행되나요?
[3,4등급 허가] 기술문서 심사대상/임상적 성능시험 자료 심사대상 → 식품의약품안전처 → 허가증
Q. 제출해야 하는 자료 무엇인가요?
[체외진단시약]
1. 이미 허가·인증 받은 제품과 비교한 자료
2. 기원·개발경위, 검출 또는 측정 원리·방법에 관한 자료
3. 국내·외 사용현황에 관한 자료
4. 원재료 및 제조방법에 관한 자료
5. 사용목적에 관한 자료
6. 저장방법과 사용기간 또는 유효기간에 관한 자료
7. 성능을 확인하기 위한 다음 각 목의 자료
· 분석적 성능시험
· 임상적 성능시험
· 품질관리 시험
· 표준물질 및 검체보관
8. 취급자 안전에 관한 자료
[체외진단장비]
1. 이미 허가·인증 받은 제품과 비교한 자료
2. 사용목적에 관한 자료
3. 작용원리에 관한 자료
4. 전기·기계적 안전에 관한 자료
5. 방사선에 관한 안전성 자료
6. 전자파안전에 관한 자료
7. 성능에 관한 자료
8. 기원 또는 발견 및 개발 경위에 대한 관한 자료
9. 임상적 성능시험에 관한 자료
10. 외국의 사용현황 등에 관한 자료
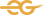 이 누리집은 대한민국 공식 전자정부 누리집입니다.
이 누리집은 대한민국 공식 전자정부 누리집입니다.




































![[대담한 정책] 대학교 학식이 단돈 1,000원인 이유? 학생들의 반응은? ‘천원의 아침밥’의 모든 것](https://www.korea.kr/newsWeb/resources/attaches/2024.04/16/2c53904642dfe8c54dc2cb98a922bcd5.jpg)
